El dogma central de la biología molecular es un concepto fundamental que forma parte de los principales planes de estudio y libros de texto de biología. Por lo tanto, los educadores pueden usar este interactivo en una amplia variedad de cursos, desde biología de primer año de bachillerato hasta asignaturas optativas de biología molecular a nivel universitario. La conexión con las técnicas genéticas y sus aplicaciones extiende su uso a los cursos de biotecnología.
La exploración de este interactivo se vincula con varias prácticas científicas, como el uso de modelos y representaciones, la participación en el cuestionamiento científico, la construcción de explicaciones basadas en evidencia y la integración del conocimiento a través de escalas y conceptos. El interactivo también enfatiza conceptos transversales clave que ayudan al estudiantado a comprender mejor las ideas centrales de la ciencia, como la importancia de la relación entre estructura y función, la escala, y las relaciones de causa y efecto.
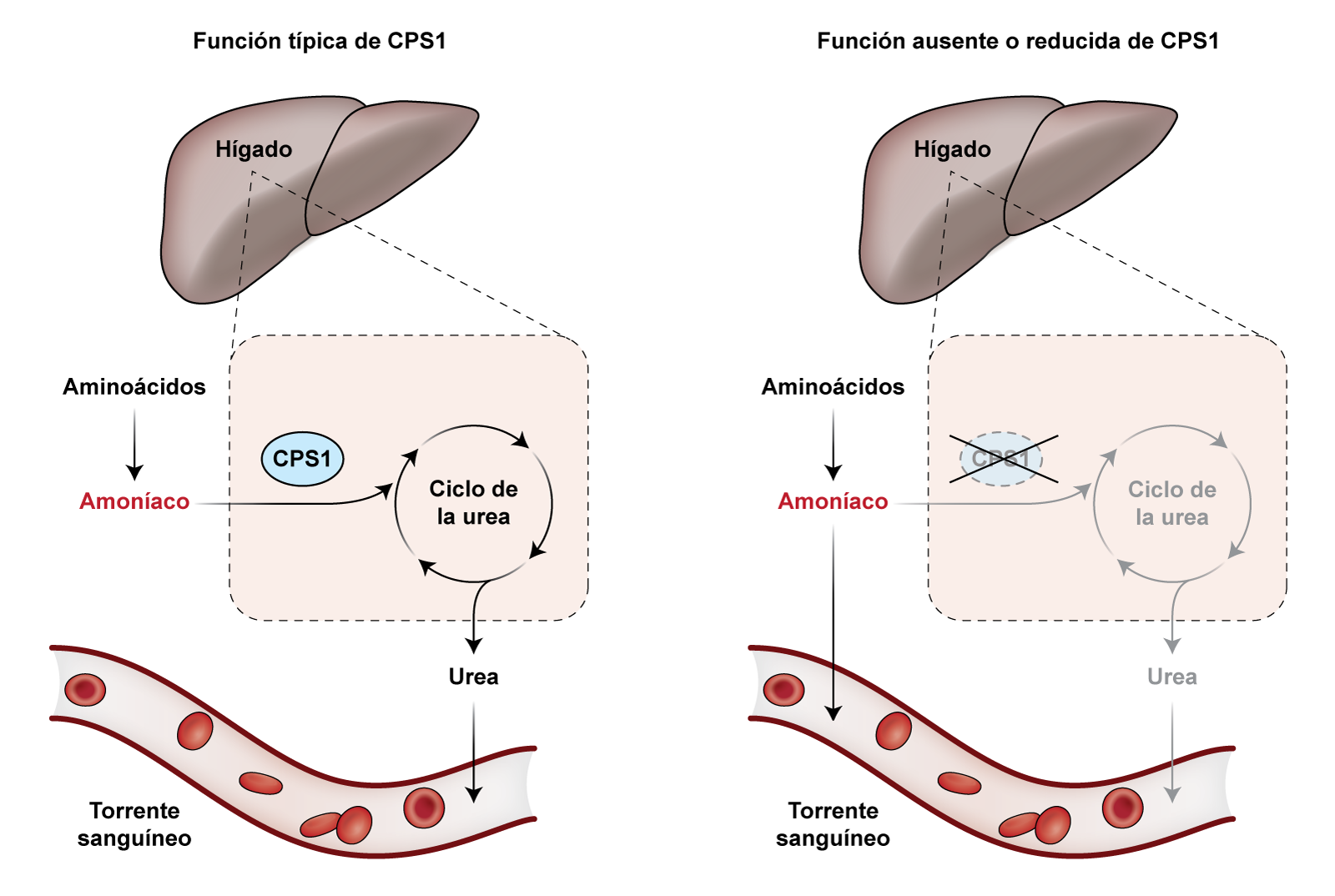
Los educadores deben tener en cuenta que el flujo de información del ADN al ARN y luego a la proteína es un proceso dinámico que implica muchas más etapas y moléculas de las que se muestran en este interactivo. Además, hay excepciones a este flujo ordenado. Por ejemplo, la comunidad científica ha descubierto que el ARN no codificante y los retrovirus son capaces de realizar una transcripción inversa, en la que la información genética fluye del ARN al ADN. Los educadores también pueden recordar a los estudiantes que, a excepción del cáncer, las enfermedades presentadas en este interactivo son monogénicas raras, causadas por mutaciones en genes individuales. Será más desafiante aplicar estas tecnologías a enfermedades más comunes causadas por una combinación de genes y factores ambientales. En la mayoría de los casos, se puede aplicar más de una estrategia terapéutica o tecnología a una misma enfermedad.
Referencias
CRISPR
Musunuru, Kiran, Sarah A. Grandinette, Xiao Wang, Taylor R. Hudson, Kevin Briseno, Anne Marie Berry, Julia L. Hacker, et al. 2025. “Patient-Specific In Vivo Gene Editing to Treat a Rare Genetic Disease.” New England Journal of Medicine 392, 22: 2235–2243. https://doi.org/10.1056/NEJMoa2504747.
AMAUROSIS CONGÉNITA DE LEBER
Bainbridge, James W. B., Alexander J. Smith, Susie S. Barker, Scott Robbie, Robert Henderson, Kamaljit Balaggan, Ananth Viswanathan, et al. 2008. “Effect of Gene Therapy on Visual Function in Leber’s Congenital Amaurosis.” New England Journal of Medicine 358, 21: 2231–2239. https://doi.org/10.1056/NEJMoa0802268.
Chacon-Camacho, Oscar Francisco, and Juan Carlos Zenteno. 2015. “Review and Update on the Molecular Basis of Leber Congenital Amaurosis.” World Journal of Clinical Cases 3, 2: 112–124. https://doi.org/10.12998/wjcc.v3.i2.112.
ENFERMEDAD DE CÉLULAS FALCIFORMES
Brendel, Christian, Swaroopa Guda, Raffaele Renella, Daniel E. Bauer, Matthew C. Canver, Young Jo Kim, Matthew M. Heeney, et al. 2016. “Lineage Specific BCL11A Knockdown Circumvents Toxicities and Reverses Sickle Phenotype.” Journal of Clinical Investigation 126, 10: 3868–3878. https://doi.org/10.1172/JCI87885.
Frangoul, Haydar, David Altshuler, M. Domenica Cappellini, Yi Shan Chen, Jennifer Domm, Brenda K. Eustace, Juergen Foell, et al. 2021. “CRISPR Cas9 Gene Editing for Sickle Cell Disease and β Thalassemia.” New England Journal of Medicine 384, 3: 252–260. https://doi.org/10.1056/NEJMoa2031054.
Orkin, Stuart H. 2025. “The Fetal to Adult Hemoglobin Switch — Mechanism and Therapy.” New England Journal of Medicine 392, 21: 2135–2149. https://doi.org/10.1056/NEJMra2405260.
ENFERMEDAD DE HUNTINGTON
Ionis Pharmaceuticals. 2015. “Safety, Tolerability, Pharmacokinetics, and Pharmacodynamics of ISIS 443139 in Patients With Early Manifest Huntington’s Disease.” Clinical trial registration NCT02519036. https://clinicaltrials.gov/ct2/show/NCT02519036.
Kordasiewicz, Holly B., Lisa M. Stanek, Edward V. Wancewicz, Curt Mazur, Melissa M. McAlonis, Kimberly A. Pytel, Jonathan W. Artates, et al. 2012. “Sustained Therapeutic Reversal of Huntington’s Disease by Transient Repression of Huntingtin Synthesis.” Neuron 74, 6: 1031–1044. https://doi.org/10.1016/j.neuron.2012.05.009.
Rawlins, Michael D., Nancy S. Wexler, Alice R. Wexler, Sarah J. Tabrizi, Ian Douglas, Stephen J. W. Evans, Liam Smeeth, et al. 2016. “The Prevalence of Huntington’s Disease.” Neuroepidemiology 46, 2: 144–153. https://doi.org/10.1159/000443738.
DISTROFIA MUSCULAR DE DUCHENNE
Emery, Alan E. H. 1991. “Population Frequencies of Inherited Neuromuscular Diseases—A World Survey.” Neuromuscular Disorders 1, 1: 19–29. https://doi.org/10.1016/0960-8966(91)90039-u.
Kinali, Maria, Virginia Arechavala-Gomeza, Lucy Feng, Sebahattin Cirak, David Hunt, Carl Adkin, Michela Guglieri, et al. 2009. “Local Restoration of Dystrophin Expression with the Morpholino Oligomer AVI 4658 in Duchenne Muscular Dystrophy: A Single-Blind, Placebo-Controlled, Dose-Escalation, Proof-of-Concept Study.” Lancet Neurology 8, 10: 918–928. https://doi.org/10.1016/S1474-4422(09)70211-X.
FIBROSIS QUÍSTICA
Kosorok, Michael R., Wen-Hsiang Wei, and Philip M. Farrell. 1996. “The Incidence of Cystic Fibrosis.” Statistics in Medicine 15, 5: 449–462. https://doi.org/10.1002/(SICI)1097-0258(19960315)15:5<449::AID-SIM173>3.0.CO;2-X.
Kuk, Kelly, and Jennifer L. Taylor-Cousar. 2015. “Lumacaftor and Ivacaftor in the Management of Patients with Cystic Fibrosis: Current Evidence and Future Prospects.” Therapeutic Advances in Respiratory Disease 9, 6: 313–326. https://doi.org/10.1177/1753465815601934.